在“碳达峰碳中和”背景下,迫切需求能源生产的可持续发展。锂离子电池(LIBs)广泛用于新能源汽车和各种电子产品中,而LIBs的有效使用时间通常只有3~5年,这意味着大量锂电池将面临退役问题。废旧LIBs正极材料中有价金属锂、镍、钴和锰的含量高于原矿[1-3],合理回收废旧LIBs中的有价金属不仅可以“变废为宝”,而且可以避免其污染水体和土壤,对人体健康造成威胁[4]。
针对废旧LIBs正极材料中有价金属的回收,目前应用较多的工艺途径主要有:1) 火法冶金,该工艺简单高效,但能耗大、成本高,且锂电池中的有机物在高温环境下会产生大量有害气体[5-6];2) 湿法冶金,该工艺处理量大,且浸出效率高、能耗低,但浸出过程会产生大量含酸或碱的废水,并且容易产生Cl2、NOx等有毒气体,造成二次污染[7-8]。
低共熔溶剂(Deep eutectic solvents, DES)是一种类离子液体,由氢键受体(HBA)和氢键供体(HBD)组成,混合物的共熔点低于任一单组分的熔点,具有良好的溶解性以及对环境友好、成本低廉、不易挥发等优点[9-10]。近年来,学者们已研究了多种用于废旧锂电池正极材料回收的DES,主要以氯化胆碱基为主[11]。TRAN等[12]采用氯化胆碱-乙二醇DES在220 ℃下对钴酸锂(LCO)正极材料浸出24 h,发现Co的浸出率高达94.1%。WANG等[13]发现氯化胆碱-尿素DES在180 ℃、浸出12 h的条件下,废旧LCO中Li和Co的浸出效率均高达95%。但由于这些DES的浸出条件较为苛刻(温度高、时间长),不利于在实际工作中推广应用,人们开始研究有机酸类DES。ROLDÁN-RUIZ等[14]发现氯化胆碱、对甲苯磺酸(PTSA)和水以摩尔比1∶1∶2制备的DES在90 ℃条件下,反应15 min就能将LCO完全溶解。但磺酸是一种很强的有机酸,具有腐蚀性和高毒性,会对操作人员的安全造成威胁,因此HBD宜选择其他有机酸。盐酸甜菜碱和盐酸胍与氯化胆碱类似,均含有Cl-,具有与镍、钴、锰等金属离子形成络合物的能力[15];相较于氯化胆碱,盐酸甜菜碱和盐酸胍本身也具有一定酸性,可以为DES提供酸性环境,从而更利于有价金属的溶解。
本研究利用盐酸甜菜碱(BeCl)、盐酸胍(GUC)代替氯化胆碱作为HBA,以酒石酸(TA)、柠檬酸(CA)两种天然、绿色、安全、温和的有机酸作为HBD制备四种DES,以废旧镍钴锰酸锂电池(NCM)正极材料中有价金属(Li、Ni、Co、Mn)浸出效果为目标,筛选出浸出率最高的DES,并以此为基础探究不同因素对废旧NCM正极材料中有价金属浸出效果的影响,通过响应面实验获得最优工艺参数,最后研究有价金属浸出机理。
1 实验
1.1 实验材料与仪器
废旧镍钴锰酸锂电池收集自市面废旧锂电池回收站。实验所用的化学品均为分析纯级,主要有盐酸甜菜碱(C5H12ClNO2)、盐酸胍(CH6ClN3)、无水柠檬酸(C6H8O7)、酒石酸(C4H6O6),实验用水为超纯水。
实验仪器主要有原子吸收分光光度计(SP-3803AA,上海光谱仪器有限公司)、恒温多头磁力搅拌器(HJ-6,金坛区西城新瑞仪器有限公司)、马弗炉(SX-4-10,沈阳市节能电炉厂)、电动离心机(80-1,常州国宇仪器制造有限公司)等。
1.2 材料预处理
将废旧电池放电、拆解获得正极片,再将正极片放入马弗炉中300 ℃焙烧去除黏结剂,利用毛刷将正极材料粉末从铝箔上刷除,获得较为纯净的废旧NCM正极材料粉末,过200目标准筛后保存备用。取适量NCM正极材料5组,用王水充分消解后测得Li、Ni、Co、Mn的全量,结果见表1。从表1可知,废旧NCM正极材料中Li、Ni、Co、Mn的摩尔比接近1.12∶0.51∶0.21∶0.28,其中Li含量略微偏高,可能是由于回收的锂电池还处于较新的状态,而新锂电池中Li的含量有时是过量的[16]。
| Element | Mass fraction/% | Molar ratio |
|---|---|---|
| Li | 7.77±0.08 | 1.120±0.012 |
| Ni | 29.63±0.40 | 0.505±0.007 |
| Co | 12.61±0.36 | 0.214±0.006 |
| Mn | 15.47±0.31 | 0.0282±0.006 |
1.3 低共熔溶剂制备
分别以盐酸甜菜碱(BeCl)、盐酸胍(GUC)为氢键受体(HBA),以酒石酸(TA)、柠檬酸(CA)为氢键供体(HBD),制备了四种低共熔溶剂(DES):BeCl-TA DES、BeCl-CA DES、GUC-TA DES、GUC-CA DES。当低共熔溶剂中水含量(质量分数)不超过42%时,DES中的氢键网状结构不会被破坏[17],故本研究各低共熔溶剂的含水量均设计为30%。
DES的具体制备方法为:称取一定质量的HBA和HBD(摩尔比为3∶4) 置于锥形瓶中,混合后加入去离子水,保持含水量为30%,在80 ℃条件下搅拌直至得到均匀透明的DES溶液,冷却至室温后保存备用。
1.4 正极材料的浸出
称取一定质量的废旧NCM正极材料粉末置于30 mL菌种瓶中,按一定固液比加入DES,密封。将密封后的菌种瓶置于恒温油浴锅中,加热至指定温度后定时定速搅拌,每组试验重复3次。除单因素实验指定条件外,其余浸出条件均为:浸出温度90 ℃,浸出时间120 min,固液比(S/L)50 g/L,搅拌速度700 r/min。浸出结束后,利用离心机固液分离,取上清液检测各金属离子浓度,使用式(1)计算金属元素的浸出率:
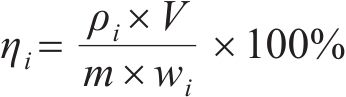
式中: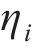
1.5 响应面优化
根据单因素实验结果可知,当浸出温度、浸出固液比和浸出时间分别为90 ℃、50 g/L、120 min时,Li、Ni、Co、Mn的浸出率已经达到较为理想的效果,兼顾节能环保,将该条件设置为因素中心水平,以Li、Ni、Co、Mn的浸出率为响应值,采用BBD(Box-Behnken design)法设计响应面实验。因素水平设计见表2。
| Level | Temperature, A /℃ | Solid-liquid ratio, B /(g·L-1) | Time, C/min |
|---|---|---|---|
| -1 | 80 | 60 | 90 |
| 0 | 90 | 50 | 120 |
| 1 | 100 | 40 | 150 |
1.6 分析方法
1) 重金属浓度测定:取1 mL浸出液于四氟乙烯消解管中,加入5 mL浓硝酸,充分振荡混合后,于石墨消解仪180 ℃消解5 h后得到无机水相,用稀硝酸(体积分数为1%)稀释后使用SP-3803AA型火焰原子吸收光谱仪检测各金属离子浓度。
2) 傅立叶红外光谱:使用Thermo Fisher Scientific Nicolet iS20型傅立叶红外光谱仪进行测定,扫描范围为500~4000 cm-1。
3) 紫外可见分光光度计(UV-vis):采用UV-vis(Alpha-1900,上海谱元仪器有限公司)对浸出液进行扫描,以BeCl-CA DES作为参比液,测试温度为室温,扫描波长范围为200~800 nm。
2 结果与讨论
2.1 DES的筛选
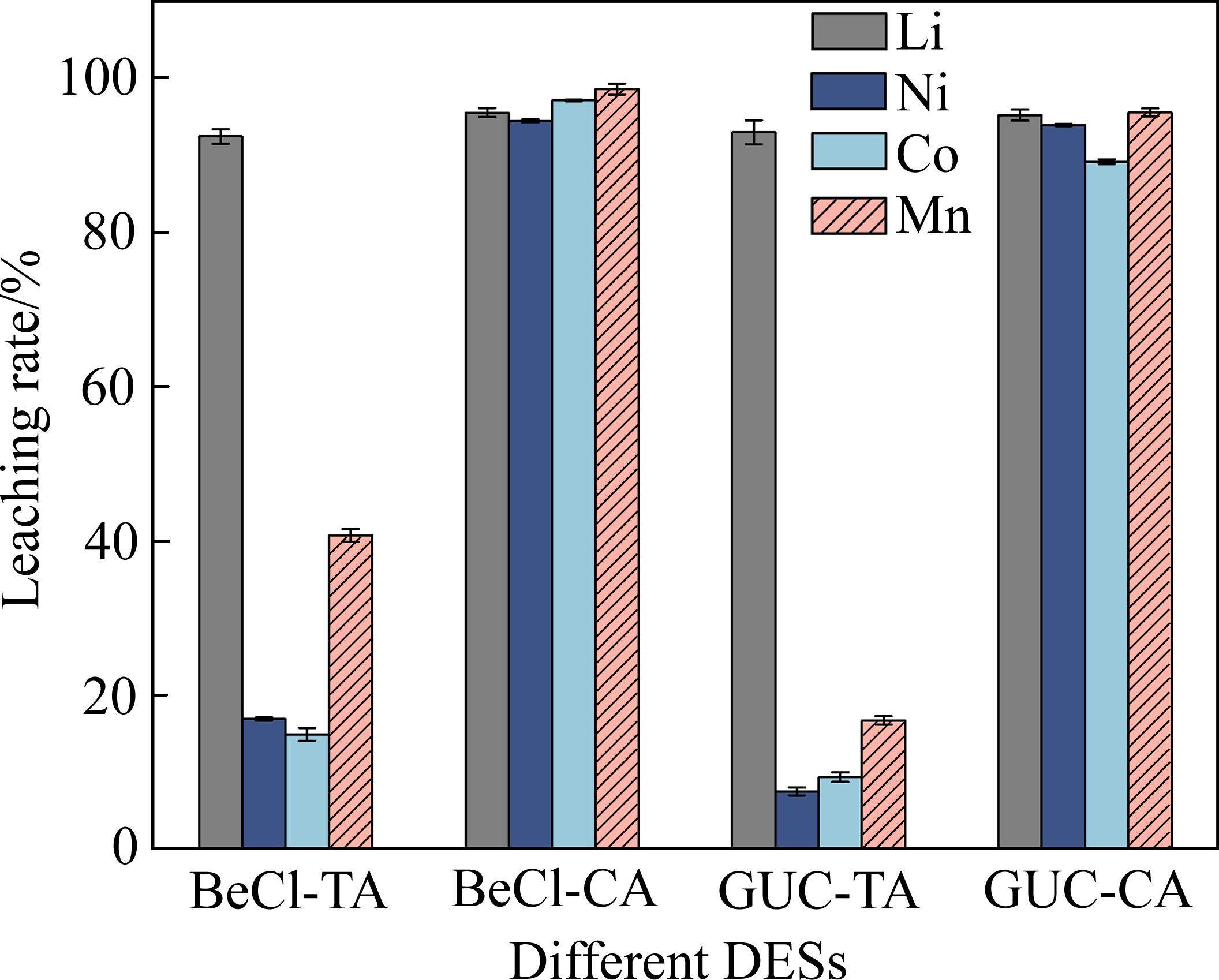
不同DES对废旧NCM正极材料中有价金属的浸出率见图1。由图1可知,以TA为HBD的两种DES仅对Li有超过90%的浸出率,对Ni、Co、Mn的浸出率均低于45%。相比而言,以CA为HBD的两种DES对四种金属浸出率均较高,其原因可能是酸性更强的CA能更好地促进Me—O键(Me为金属)的断裂和Men+的还原,从而更有利于金属的浸出[15, 18-19]。在相同(90 ℃、50 g/L、120 min)的反应条件下,BeCl-CA DES对Li、Ni、Co、Mn的浸出率分别为95.49%、94.41%、97.05%、98.52%,均高于GUC-CA DES的95.16%、93.88%、89.11%、95.52%。另外,BeCl比GUC更为廉价易得,因此,从浸出率和成本综合考虑,选取BeCl-CA DES为后续研究对象。
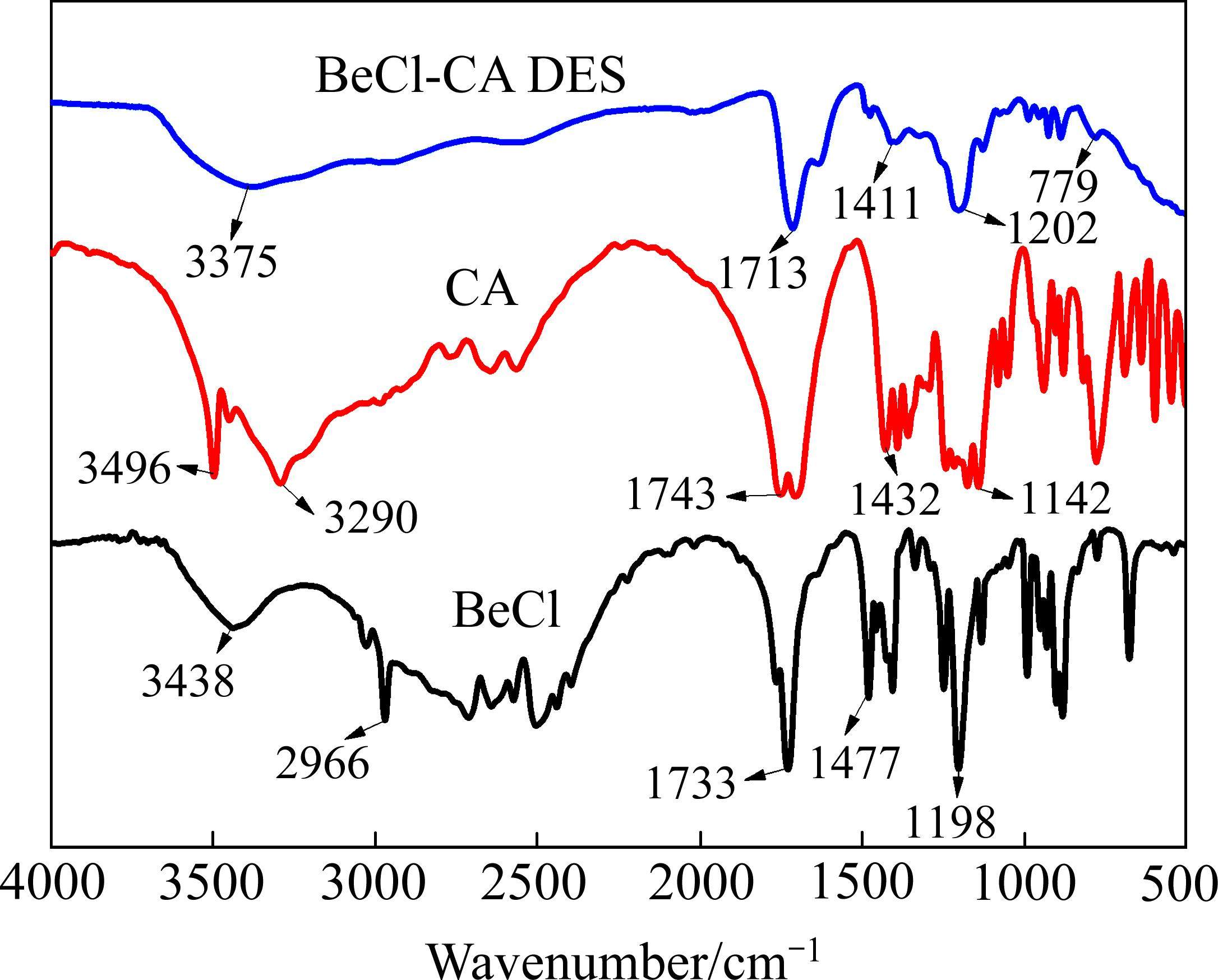
对BeCl、CA和BeCl-CA DES进行红外光谱检测,结果如图2所示。由图2可知,BeCl的红外光谱中3438 cm-1处为O—H基团的伸缩振动,2966 cm-1处为C—H的伸缩振动,1733 cm-1处为C=O伸缩振动,1477 cm-1处为C—H弯曲振动,1198 cm-1处为C—N伸缩振动。CA的红外光谱中3496 cm-1和3290 cm-1处为O—H伸缩振动,1743 cm-1处为C=O伸缩振动,1432 cm-1处为COO—对称弯曲振动,1142 cm-1处为C—O伸缩振动。从BeCl-CA的红外光谱可以发现,BeCl-CA中O—H伸缩振动吸收峰位于3375 cm-1处,较CA和BeCl对应位置的峰变宽、强度变低并向低波数方向移动,说明BeCl-CA中形成了氢键,并且O—H基团可能参与了BeCl和CA之间更为广泛的氢键网络的形成[20]。
2.2 正极材料浸出因素影响
1) 浸出温度的影响
浸出温度对金属浸出率的影响见图3(a)。由图3(a)可知,温度对金属浸出率影响很大,当浸出温度为60 ℃时,Li、Ni、Co、Mn的浸出率分别为80.48%、66.66%、68.68%、68.70%;当浸出温度升高至90 ℃时,Li、Ni、Co、Mn的浸出率分别提高至95.15%、94.64%、97.05%、98.19%;当温度继续增加至120 ℃时,浸出率略有提升。较高的浸出温度不仅可以增加柠檬酸的电离,而且还可以降低DES的黏度,促进溶液中各种离子间的碰撞,从而提高反应速度[21]。从节约能耗角度考虑,选取90 ℃作为后续浸出温度。
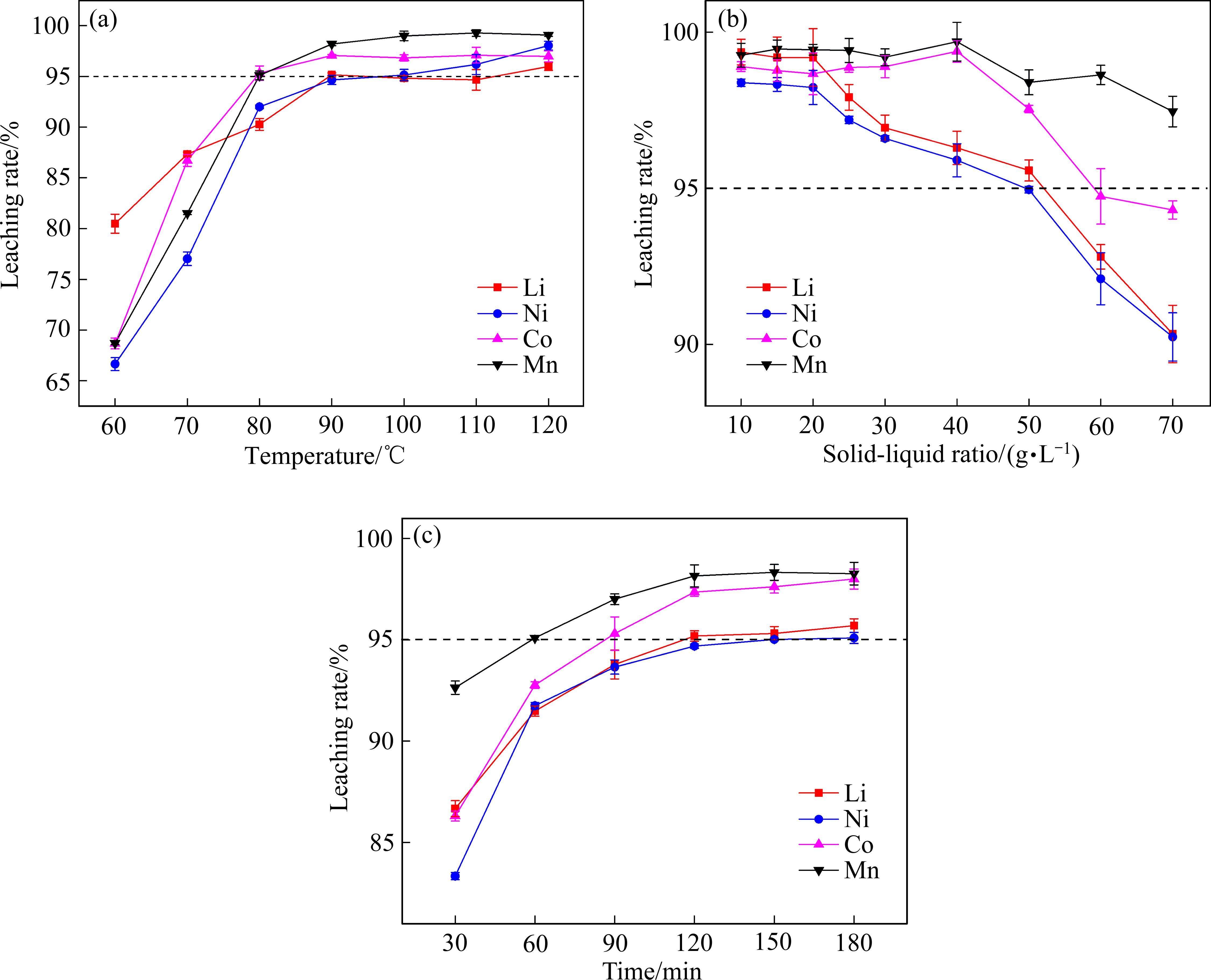
2) 固液比的影响
固液比对金属浸出率的影响见图3(b)。由图3(b)可知,在固液比不高于20 g/L时,Li、Ni、Co、Mn的浸出率基本保持稳定,分别为99.19%、98.23%、98.67%、99.44%;当固液比增加至50 g/L时,Li、Ni、Co、Mn的浸出率分别降低至95.57%、94.96%、97.54%、98.39%;当固液比超过50 g/L时,除Mn外,Li、Ni、Co的浸出率开始急剧下降。这是由于随着废旧NCM正极材料投加量增加,固体颗粒与DES的接触面减小,液体流动性变差,不利于金属离子的传质,限制了浸出反应的进行。虽然固液比为20 g/L时,各金属元素的浸出率均超过98%,但DES的消耗量较大,并且极有可能存在浸出能力剩余的情况;当固液比为50 g/L时,尽管浸出率略有下降,但是仍具有较为理想的浸出效果。因此,为了保证高浸出效率和低经济成本,选取50 g/L为后续反应固液比。
3) 浸出时间的影响
浸出时间对浸出率的影响见图3(c)。由图3(c)可知,当浸出时间从30 min延长至120 min时,Li、Ni、Co、Mn的浸出率分别从86.67%、83.34%、86.30%、92.64%提高至95.19%、94.69%、97.36%、98.15%;继续延长至180 min时,Li、Ni、Co、Mn的浸出率几乎保持稳定。从节约时间考虑,选择120 min为最佳浸出时间。
2.3 浸出条件优化
利用Design-Expert 13对响应面实验结果进行回归分析,结果见表3。
| Element | Item | Source | R2 | ||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| Model | A | B | C | AB | AC | BC | A2 | B2 | C2 | Lack of fit | |||
| Li | Mean square | 7.60 | 19.00 | 25.24 | 8.69 | 0.14 | 0.21 | 1.05 | 8.43 | 1.49 | 2.92 | 0.05 | 0.9879 |
| P-value | <0.0001 | <0.0001 | <0.0001 | <0.0001 | 0.3082 | 0.2298 | 0.0210 | <0.0001 | 0.0096 | 0.0017 | 0.8303 | ||
| Ni | Mean square | 5.23 | 14.55 | 21.68 | 3.92 | 0.006 | 0.003 | 0.065 | 4.48 | 1.55 | 0.32 | 0.10 | 0.9819 |
| P-value | <0.0001 | <0.0001 | <0.0001 | 0.0008 | 0.8268 | 0.8803 | 0.4925 | 0.0005 | 0.0096 | 0.1551 | 0.5818 | ||
| Co | Mean square | 6.77 | 17.46 | 27.57 | 5.73 | 0.042 | 0.216 | 1.06 | 4.20 | 2.44 | 1.37 | 0.17 | 0.9874 |
| P-value | <0.0001 | <0.0001 | <0.0001 | 0.0002 | 0.5575 | 0.2052 | 0.0175 | 0.0005 | 0.0022 | 0.0097 | 0.2043 | ||
| Mn | Mean square | 4.29 | 17.02 | 4.44 | 4.34 | 1.70 | 0.25 | 0.245 | 8.85 | 0.049 | 1.34 | 0.17 | 0.9737 |
| P-value | 0.0001 | <0.0001 | 0.0009 | 0.0010 | 0.0118 | 0.2364 | 0.2407 | 0.0001 | 0.5840 | 0.0199 | 0.3923 | ||
从表3中可以看出,Li、Ni、Co、Mn回归方程显著性检验的P≤0.0001,表明四个回归方程均具有显著性。四个回归方程的决定系数R2均高于0.97,表明拟合效果较好。四个模型实验信噪比(Adeq precision)均大于4,表明所设计的实验和分析得到的回归方程模型是合理的。另外,A(反应温度)、B(固液比)、C(反应时间)均对Li、Ni、Co、Mn浸出有显著影响(P≤0.001),其中对Li、Ni、Co的影响排序为:B(固液比)>A(浸出温度)>C(浸出时间);对Mn的影响排序则为:A(浸出温度)>B(固液比)≈C(浸出时间)。
图4所示为各因素的交互影响分析结果。从图4和表3可以看出,B和C的交互作用对Li、Co的浸出率影响显著(PBC<0.05),A和B的交互作用对Mn的浸出率影响显著(PAB<0.05),A、B、C两两交互作用对Ni的浸出率影响均不显著。总体上看,Li、Ni、Co、Mn的浸出率随着A、C的增大和B的减小而增大。
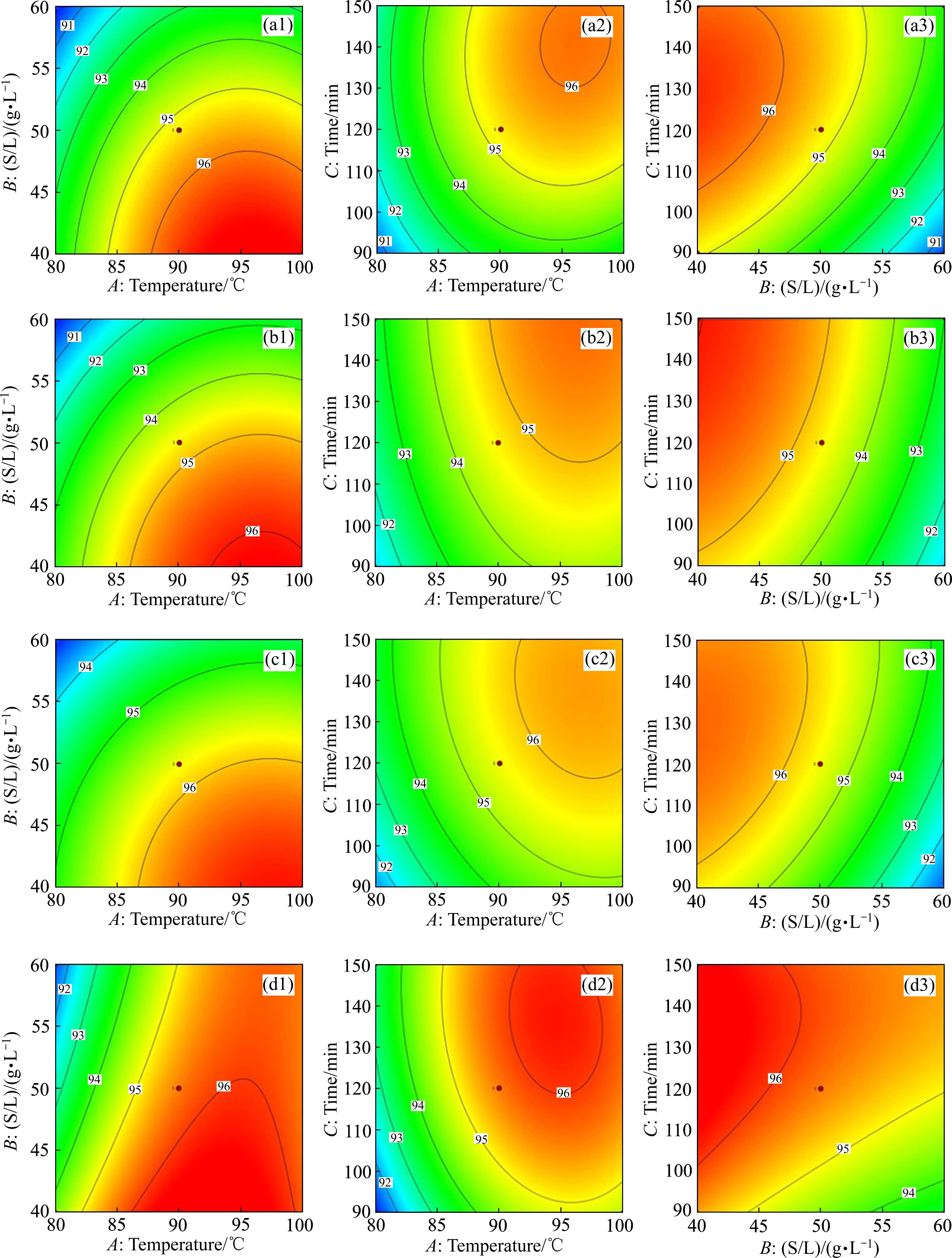
经回归方程计算得到BeCl-CA DES浸出废旧NCM正极材料中有价金属的最佳条件为:反应温度97.75 ℃、固液比40 g/L、反应时间123.89 min。在反应温度95 ℃、固液比40 g/L、反应时间125 min的条件下进行验证,结果见表4。由表4可知,三次重复验证实验中Li、Ni、Co、Mn的浸出率平均值分别为97.23%、95.99%、99.31%、99.24%,与理论预测值均十分接近,表明该预测模型可靠。
| Value | Factor | Leaching rate/% | ||||||
|---|---|---|---|---|---|---|---|---|
| Temperature/℃ | (S/L)/(g·L-1) | Time/min | Li | Ni | Co | Mn | ||
| Predicted | 97.751 | 40.000 | 123.886 | 97.03 | 96.24 | 99.27 | 99.30 | |
| Measured | 95 | 40 | 125 | 97.10 | 95.71 | 98.90 | 99.63 | |
| 96.98 | 96.35 | 99.74 | 98.78 | |||||
| 97.61 | 95.92 | 99.28 | 99.30 | |||||
本研究与其他研究成果的比较如表5所示。由表5可知,已有研究主要以浸出难度更小的LCO为研究对象,且尽管部分DES对废弃LIBs正极材料中金属的浸出率已接近100%,但其实验条件中要么浸出温度较高,要么固液比较小,亦或是浸出时间较长。本实验BeCl-CA DES与ChCl基DES相比,BeCl携带的羧基具有更强的与空轨道金属离子结合的能力[22],使得BeCl-CA DES在用于废旧NCM正极材料浸出时所需浸出时间较短(125 min)、温度相对温和(95 ℃)、固液比(1 g/25 g)也不高,实现了废旧NCM正极材料中有价金属的高效浸出。
| DES | Material | Condition | Leaching rate/% | Ref. | ||
|---|---|---|---|---|---|---|
| Temperature/℃ | (S/L)/(g·g-1) | Time/h | ||||
| n(BeCl)∶n(CA)=3∶4 | NCM | 95 | 1/25 | 2 | Li: 97.2; Co: 99.3; Ni: 96.0; Mn: 99.2 | This work |
| n(ChCl)∶n(TA)=1∶1 | 70 | 1/50 | 12 | Li: 96.0; Co: 97.1; Ni: 98.0; Mn: 96.7 | [23] | |
| n(BeCl)∶n(FA)=1∶9 | 140 | 1/50 | 6 | Li: 98.0; Co: 99.2; Ni: 92.4; Mn: 96.0 | [24] | |
n(ChCl)∶n(BSA)∶n(EG)= 1∶1∶2 | LCO | 90 | 1/50 | 2 | Li: 99.0; Co: 98.0 | [20] |
n(ChCl)∶n(SA)∶n(EG)= 1∶1∶1 | 140 | 1/300 | 16 | Li: 99.6; Co: 99.6 | [25] | |
| n(ChCl)∶n(OA)=1∶1 | 120 | 1/50 | 12 | Li: 96.1; Co: 96.3 | [26] | |
| n(ChCl)∶n(OA)=1∶1 | 110 | 1/50 | 2.5 | Li: 100; Co: 100 | [27] | |
n(ChCl)∶n(PTSA)∶n(H2O)= 1∶1∶2 | 90 | 1/50 | 0.25 | Li: 100; Co: 100 | [14] | |
| n(ChCl)∶n(FA)=1∶2 | 90 | 1/50 | 12 | Li: 99.8; Co: 99.1 | [28] | |
| n(ChCl)∶n(ACA)=1∶2 | 90 | 1/50 | 12 | Li: 60.0; Co: 30.0 | [28] | |
| n(ChCl)∶n(EG)=1∶2 | 180 | 1/50 | 24 | Li: 89.8; Co: 50.3 | [12] | |
| n(ChCl)∶n(Urea)=1∶2 | 160 | 1/50 | 12 | Li: 61.2; Co: 64.2 | [13] | |
| 180 | 1/50 | 12 | Li: 94.7; Co: 97.9 | |||
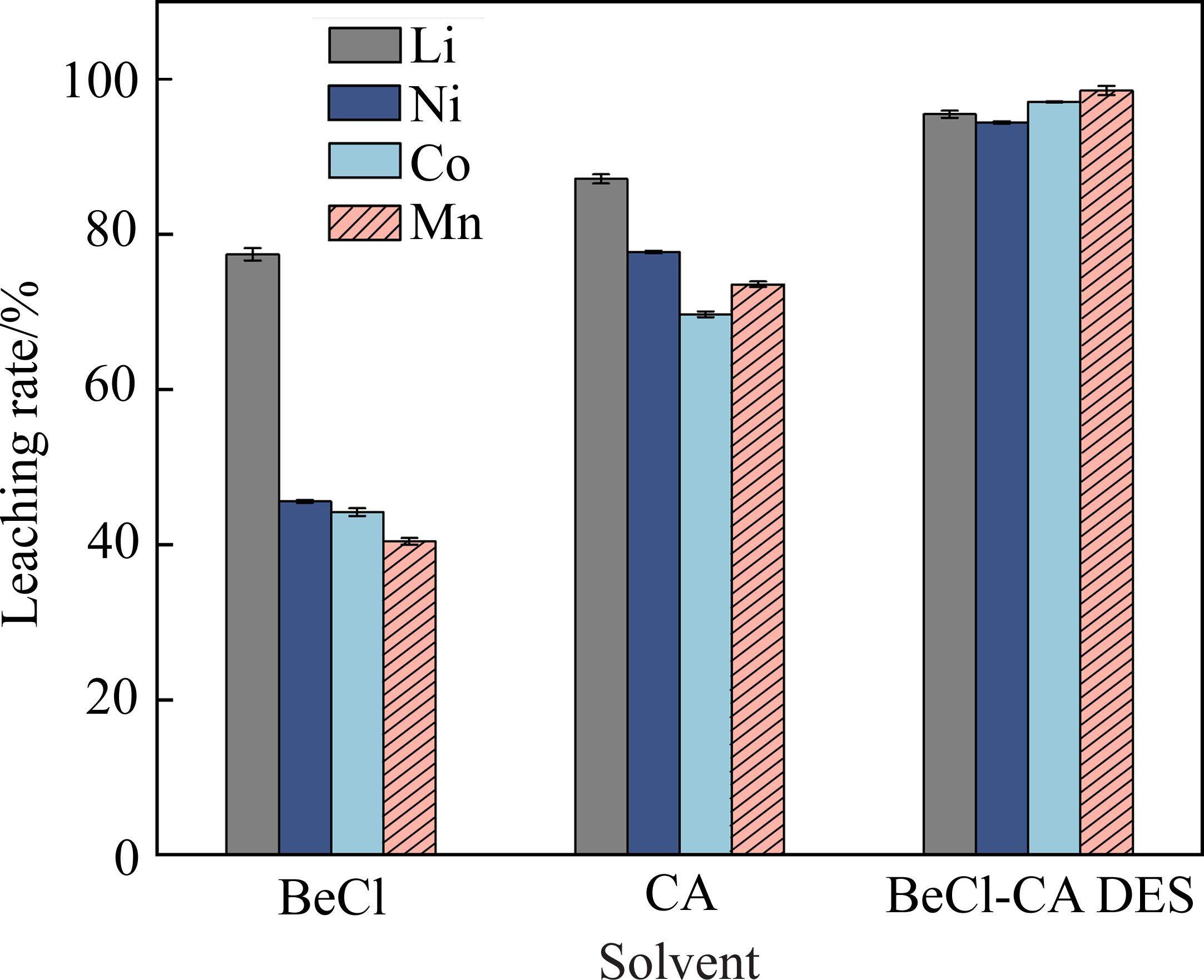
2.4 浸出机理分析
分别使用BeCl、CA和BeCl-CA DES对废旧NCM正极材料进行浸出,结果如图5所示。由图5可以看出,BeCl和CA本身对废旧NCM正极材料有一定的浸出效果,并且Li的浸出率明显高于Ni、Co、Mn,这是因为BeCl和CA都可以电离出氢离子使浸出液呈酸性;另外,研究表明废旧NCM正极材料具有α-NaFeO2晶体结构,属于R
为进一步了解浸出过程,测定了不同浸出时间浸出液的紫外光谱(由于200~550 nm范围内无可用特征吸收峰,因此仅展示550~800 nm范围内的扫描谱线),如图6所示。随着浸出时间的增加,浸出液的紫外可见光谱峰强度也逐渐增加,这与图3(c)的浸出规律一致。
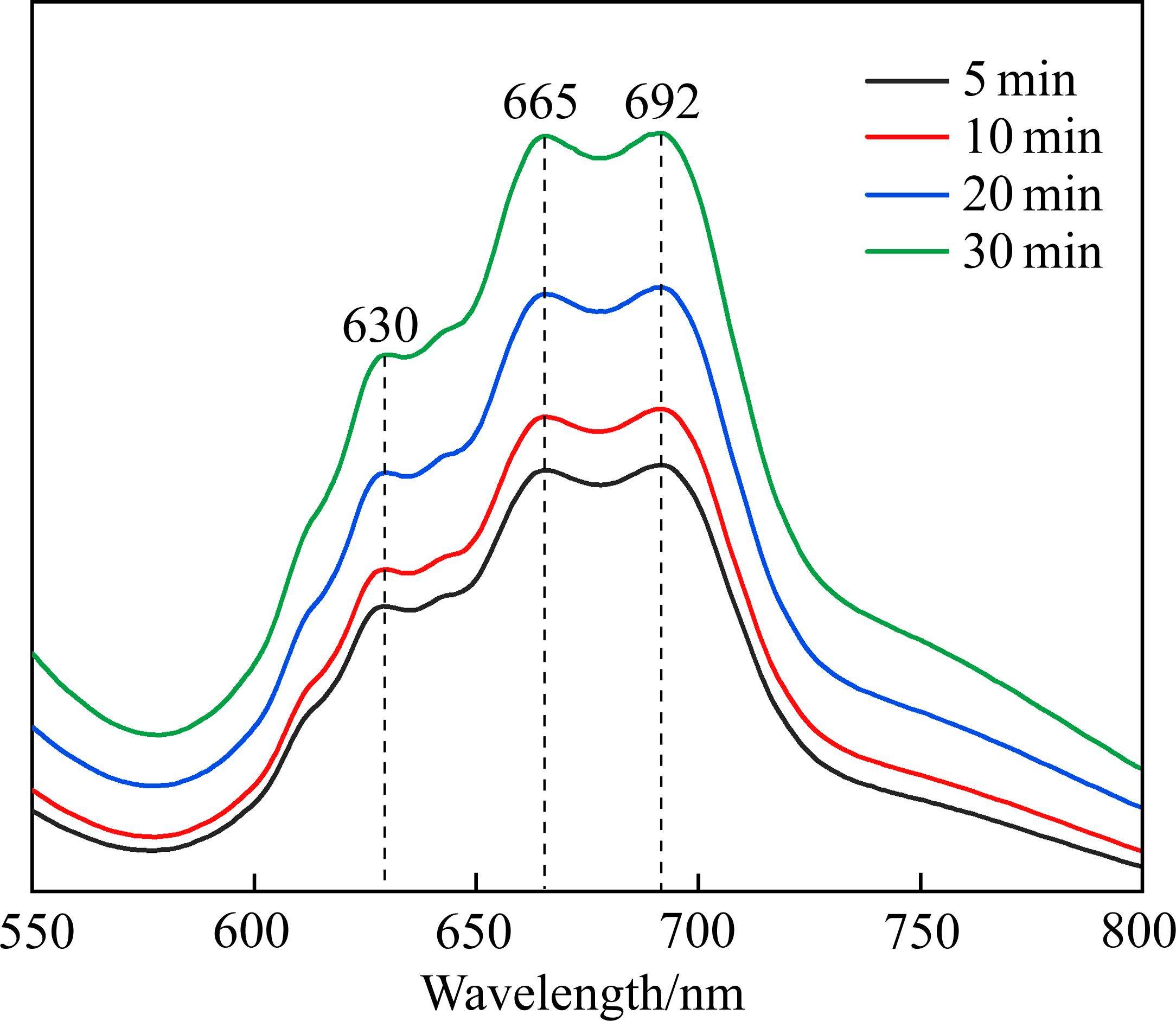
在630 nm、665 nm、692 nm三处出现的吸收峰为[CoCl4]2-典型的三重吸收峰,证明DES中携带的Cl-可以与正极材料中的Co形成配合物。在废旧NCM正极材料中Co以Co3+形式存在,而在[CoCl4]2-中Co是以Co2+形式存在的,说明DES在浸出废旧NCM正极材料过程中发生了还原反应;而柠檬酸具有还原高价金属的能力[31],因此推测该还原反应与柠檬酸有关。
综上所述,DES是靠酸性、还原性和Cl-的强配位三种作用协同浸出废旧NCM正极材料中的金属元素,具体反应过程为:DES中电离出来的H+可以取代废旧NCM正极材料层状结构中的锂,使得过渡金属暴露,并与晶体中的氧发生反应,进而破坏Me—O键,使得过渡金属离子溶解;高价金属离子可被柠檬酸还原,同时与具有强配位能力的Cl-形成[MeCl4]2-,以此促使浸出反应持续进行。浸出过程可能发生的反应方程如下[24, 32]:
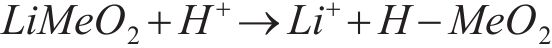
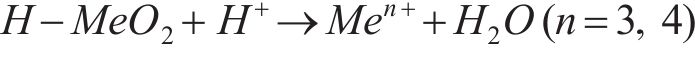
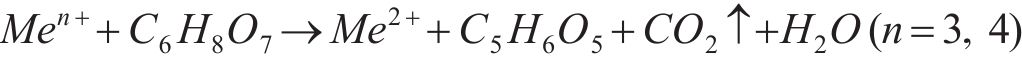
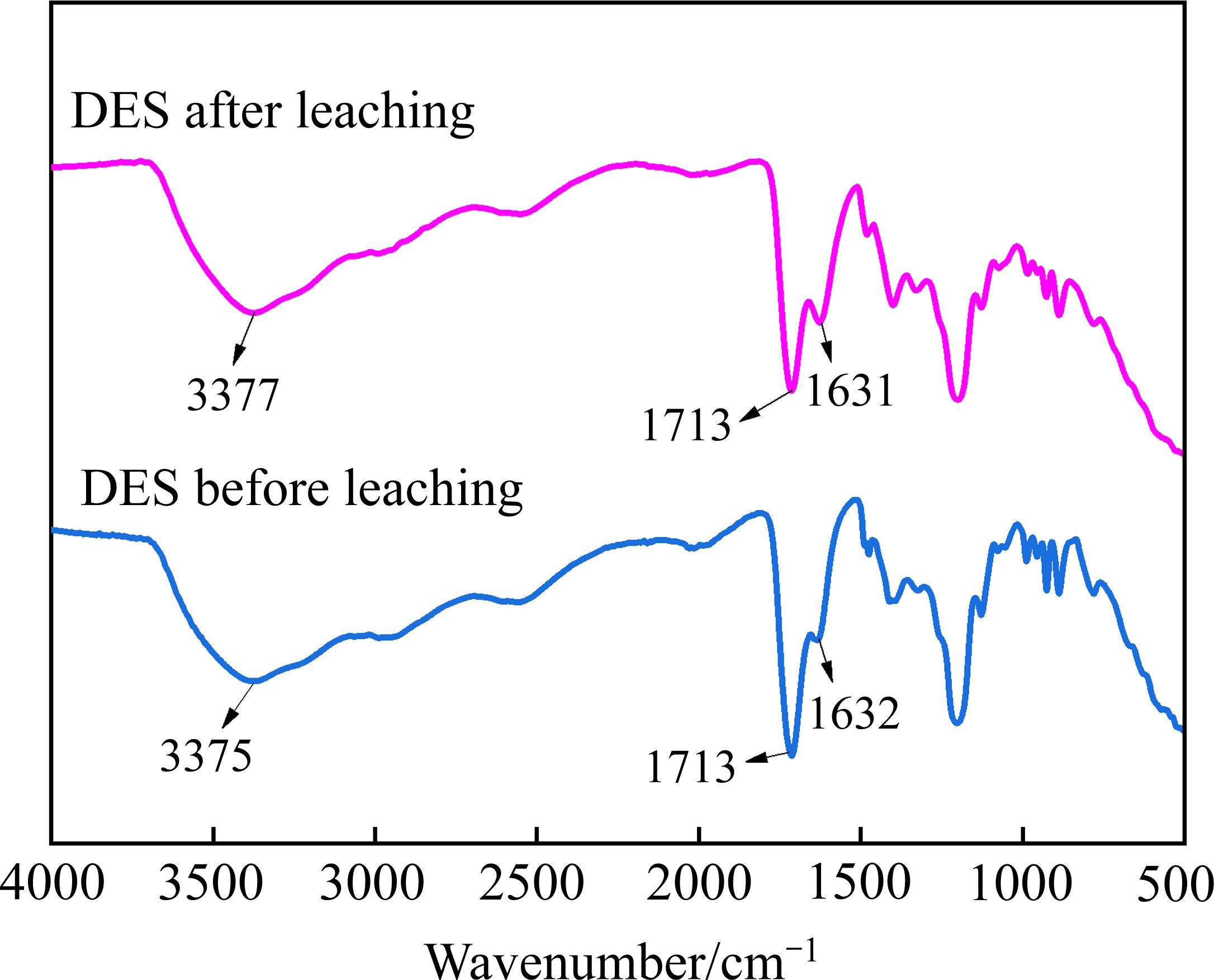
图7所示为浸出前后DES的红外光谱。由图7可知,在浸出后DES的红外光谱中,3377 cm-1处O—H的吸收峰强度略有减弱,这与DES中的氢键供体参与金属的还原反应有关,伴随氢键供体的减少,O—H吸收峰强度减弱[32]。此外,在1631 cm-1左右出现的小峰比浸出前DES的红外光谱更强,该峰对应的是羧酸盐中—COO—的拉伸振动,说明在浸出过程中可能会生成羧酸盐[23, 33],印证了柠檬酸参与还原反应的猜想。除此之外,浸出前后DES的其他官能团未发生明显变化,表明BeCl-CA DES在浸出金属前后的结构基本保持稳定。
2.5 浸出动力学研究
废旧NCM正极材料在DES中的浸出过程可分三个阶段:1) 液相的DES通过液膜层向废旧NCM正极材料表面扩散;2) DES与废旧NCM正极材料表面接触并进行化学反应;3) 废旧NCM正极材料表面生成产物并扩散到液相主体。该反应过程可用未反应核收缩模型来描述,即废旧NCM正极材料的浸出过程主要受扩散反应和表面化学反应的影响,式(6)和(7)为相应的浸出动力学方程。
扩散反应:
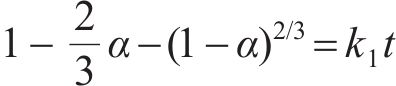
表面化学反应:
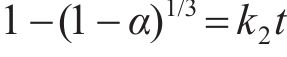
式中: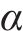
将各金属离子在不同温度下的浸出结果代入动力学方程进行拟合,结果见表6。拟合结果表明,Li、Ni、Co、Mn在两个动力学方程中的拟合曲线均具有良好的线性关系(R2>0.97),即废旧NCM正极材料在DES中的浸出过程受到扩散反应和表面化学反应的双重控制。但由于废旧NCM正极材料在DES中的整个浸出过程是在剧烈搅拌下进行的(700 r/min),因此,外部扩散阻力的影响相对较小[34-35],浸出过程的主要控制步骤为表面化学反应。
| Equation | Temperature/ ℃ | Li | Ni | Co | Mn | |||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|
| k | R2 | k | R2 | k | R2 | k | R2 | |||||
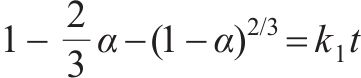 | 60 | 0.9913 | 0.9934 | 0.9810 | 0.9963 | 0.9913 | 0.9934 | 0.9810 | 0.9963 | |||
| 70 | 0.9971 | 0.9948 | 0.9583 | 0.9852 | 0.9971 | 0.9948 | 0.9583 | 0.9852 | ||||
| 80 | 0.9963 | 0.9833 | 0.9845 | 0.9892 | 0.9963 | 0.9833 | 0.9845 | 0.9892 | ||||
| 90 | 0.9886 | 0.9833 | 0.9893 | 0.9983 | 0.9886 | 0.9833 | 0.9893 | 0.9983 | ||||
 | 60 | 0.9993 | 0.9976 | 0.9747 | 0.9994 | 0.9993 | 0.9976 | 0.9747 | 0.9994 | |||
| 70 | 0.9977 | 0.9964 | 0.9552 | 0.9766 | 0.9977 | 0.9964 | 0.9552 | 0.9766 | ||||
| 80 | 0.9962 | 0.9824 | 0.9860 | 0.9897 | 0.9962 | 0.9824 | 0.9860 | 0.9897 | ||||
| 90 | 0.9911 | 0.9858 | 0.9938 | 0.9903 | 0.9911 | 0.9858 | 0.9938 | 0.9903 | ||||
3 结论
1) 制备了四种新型的低共熔溶剂:BeCl-TA DES、BeCl-CA DES、GUC-TA DES、GUC-CA DES,其中,BeCl-CA DES对废旧NCM正极材料中有价金属的浸出率最高。
2) 探究了不同因素对废旧NCM正极材料中Li、Ni、Co、Mn的浸出率的影响,结果表明,浸出温度、浸出时间以及固液比对浸出率均有显著影响,且浸出温度和固液比的影响总体上强于浸出时间。在最优反应条件下(浸出温度为95 ℃,固液比为40 g/L,浸出时间为125 min),废旧NCM正极材料中Li、Ni、Co、Mn的浸出率分别为97.23%、95.99%、99.31%、99.24%。
3) 通过对单一组分浸出结果、UV-vis光谱图及红外光谱分析表明,BeCl-CA DES浸出废旧NCM正极材料时,BeCl-CA DES中电离的H+在取代锂后,继续破坏Me—O键,溶出金属离子,且由于DES中柠檬酸的还原作用,高价金属离子被还原并与Cl-形成[MeCl4]2-,完成浸出过程。浸出动力学研究表明,该浸出过程主要受表面化学控制。
李堂姝, 刘建, 兰伟伟, 等. BeCl-CA DES回收废旧NCM正极材料中的有价金属[J]. 中国有色金属学报, 2025, 35(1): 258-269. DOI: 10.11817/j.ysxb.1004.0609.2024-45152
LI Tangshu, LIU Jian, LAN Weiwei, et al. Recovery of valuable metals from cathode materials of spent NCM lithium-ion batteries with BeCl-CA DES[J]. The Chinese Journal of Nonferrous Metals, 2025, 35(1): 258-269. DOI: 10.11817/j.ysxb.1004.0609.2024-45152

